- La radiación ionizante es un tipo de energía liberada por los átomos en forma de ondas electromagnéticas o partículas.
- Las personas están expuestas a fuentes naturales de radiación ionizante, como el suelo, el agua o la vegetación, y a fuentes artificiales, tales como los rayos X y algunos dispositivos médicos.
- Las radiaciones ionizantes tienen muchas aplicaciones beneficiosas en la medicina, la industria, la agricultura y la investigación.
- A medida que aumenta el uso de las radiaciones ionizantes también lo hacen los posibles peligros para la salud si no se utilizan o contienen adecuadamente.
- Cuando las dosis de radiación superan determinados niveles pueden tener efectos agudos en la salud, tales como quemaduras cutáneas o síndrome de irradiación aguda.
- Las dosis bajas de radiación ionizante pueden aumentar el riesgo de efectos a largo plazo, tales como el cáncer.
¿Qué es la radiación ionizante?
La radiación ionizante es un tipo de energía liberada por los átomos en forma de ondas electromagnéticas (rayos gamma o rayos X) o partículas (partículas alfa y beta o neutrones). La desintegración espontánea de los átomos se denomina radiactividad, y la energía excedente emitida es una forma de radiación ionizante. Los elementos inestables que se desintegran y emiten radiación ionizante se denominan radionúclidos.
Cada radionúclido se caracteriza por el tipo de radiación que emite, la energía de la radiación y su semivida.
La actividad, utilizada como medida de la cantidad de un radionúclido, se expresa en una unidad llamada becquerel (Bq): un becquerel corresponde a una desintegración por segundo. La semivida es el tiempo necesario para que la actividad de un radionúclido disminuya por la desintegración a la mitad de su valor inicial. La semivida de un elemento radiactivo es el tiempo que tarda la mitad de sus átomos en desintegrarse, y puede variar desde una fracción de segundo a millones de años (por ejemplo, el yodo 131 tiene una semivida de 8 días mientras que el carbono 14 tiene una semivida de 5730 años).
Fuentes de radiación
Las personas están expuestas a la radiación natural a diario. La radiación natural proviene de muchas fuentes, como los más de 60 materiales radiactivos naturales presentes en el suelo, el agua y el aire. El radón es un gas natural que emana de las rocas y la tierra y es la principal fuente de radiación natural. Diariamente inhalamos e ingerimos radionúclidos presentes en el aire, los alimentos y el agua.
Asimismo, estamos expuestos a la radiación natural de los rayos cósmicos, especialmente a gran altura. Por término medio, el 80% de la dosis anual de radiación de fondo que recibe una persona procede de fuentes de radiación naturales, terrestres y cósmicas. Los niveles de la radiación de fondo varían debido a diferencias geológicas. En determinadas zonas la exposición puede ser más de 200 veces mayor que la media mundial.
La exposición humana a la radiación proviene también de fuentes artificiales que van desde la generación de energía nuclear hasta el uso médico de la radiación para fines diagnósticos o terapéuticos. Hoy día, las fuentes artificiales más comunes de radiación ionizante son los aparatos de rayos X y otros dispositivos médicos.
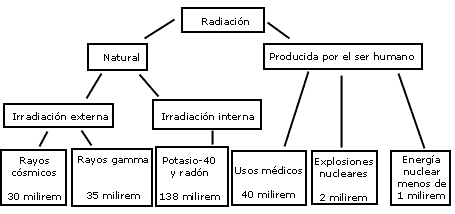
Tipos de exposición
La exposición a la radiación puede ser interna o externa, y puede tener lugar por diferentes vías.
La exposición interna a la radiación ionizante se produce cuando un radionúclido es inhalado, ingerido o entra de algún otro modo en el torrente sanguíneo (por ejemplo, inyecciones o heridas). La exposición interna cesa cuando el radionúclido se elimina del cuerpo, ya sea espontáneamente (por ejemplo, en los excrementos) o gracias a un tratamiento.
La contaminación externa se puede producir cuando el material radiactivo presente en el aire (polvo, líquidos, aerosoles) se deposita sobre la piel o la ropa. Generalmente, este tipo de material radiactivo puede eliminarse del organismo por simple lavado.La exposición a la radiación ionizante también puede resultar de la irradiación externa (por ejemplo, la exposición médica a los rayos X). La irradiación externa se detiene cuando la fuente de radiación está blindada o la persona sale del campo de irradiación.
Efectos de las radiaciones ionizantes en la salud
El daño que causa la radiación en los órganos y tejidos depende de la dosis recibida, o dosis absorbida, que se expresa en una unidad llamada gray (Gy). El daño que puede producir una dosis absorbida depende del tipo de radiación y de la sensibilidad de los diferentes órganos y tejidos.
El sievert (Sv) es una unidad de dosis de radiación ponderada, también llamada dosis efectiva. Es una manera de medir la radiación ionizante en términos de su potencial para causar daño. El sievert tiene en cuenta el tipo de radiación y la sensibilidad de los tejidos y órganos. El sievert es una unidad muy grande, por lo que resulta más práctico utilizar unidades menores, como el milisievert (mSv) o el microsievert (μSv). Hay 1000 μSv en 1 mSv, y 1000 mSv en 1 Sv. Además de utilizarse para medir la cantidad de radiación (dosis), también es útil para expresar la velocidad a la que se entrega esta dosis (tasa de dosis), por ejemplo en μSv/hora o mSv/año.
Más allá de ciertos umbrales, la radiación puede afectar el funcionamiento de órganos y tejidos, y producir efectos agudos tales como enrojecimiento de la piel, caída del cabello, quemaduras por radiación o síndrome de irradiación aguda. Estos efectos son más intensos con dosis más altas y mayores tasas de dosis. Por ejemplo, la dosis liminar para el síndrome de irradiación aguda es de aproximadamente 1 Sv (1000 mSv).
Si la dosis es baja o se recibe a lo largo de un periodo amplio (tasa de dosis baja) hay más probabilidades de que las células dañadas se reparen con éxito. Aun así, pueden producirse efectos a largo plazo si el daño celular es reparado, pero incorpora errores, transformando una célula irradiada que todavía conserva su capacidad de división. Esa transformación puede producir cáncer pasados años o incluso decenios. No siempre se producen efectos de este tipo, pero la probabilidad de que ocurran es proporcional a la dosis de radiación. El riesgo es mayor para los niños y adolescentes, ya que son mucho más sensibles que los adultos a la exposición a la radiación.
Los estudios epidemiológicos de poblaciones expuestas a la radiación (sobrevivientes de la bomba atómica o pacientes sometidos a radioterapia) muestran un aumento significativo del riesgo de cáncer con dosis superiores a 100 mSv.
La radiación ionizante puede producir daños cerebrales en el feto tras la exposición prenatal aguda a dosis superiores a 100 mSv entre las 8 y las 15 semanas de gestación y a 200 mSv entre las semanas 16 y 25. Los estudios en humanos no han demostrado riesgo para el desarrollo del cerebro fetal con la exposición a la radiación antes de la semana 8 o después de la semana 25. Los estudios epidemiológicos indican que el riesgo de cáncer tras la exposición fetal a la radiación es similar al riesgo tras la exposición en la primera infancia.
Exposición a la radiación en emergencias nucleares
Durante los accidentes en plantas de energía nuclear puede liberarse material radiactivo al medio ambiente. Los radionúclidos más preocupantes para la salud humana son el yodo y el cesio.
Durante la respuesta a esas emergencias es probable que se produzca exposición ocupacional, interna o externa, de los rescatadores, del personal de primero auxilios y trabajadores de las centrales nucleares. Las dosis de radiación pueden ser suficientemente altas como para causar efectos agudos, tales como quemaduras en la piel o síndrome de irradiación aguda.
Quienes viven muy cerca de centrales nucleares pueden sufrir exposición externa a los radionúclidos presentes en una nube radiactiva o depositados en el suelo. También se pueden contaminar externamente por partículas radiactivas depositadas en la piel o la ropa. También puede haber exposición interna si los radionúclidos se inhalan, ingieren o introducen en heridas abiertas.La población en general no es probable que se vea expuesta a dosis suficientemente altas para causar efectos agudos, pero sí a dosis bajas que podrían aumentar el riesgo de efectos a largo plazo, como el cáncer. El consumo de agua o alimentos contaminados contribuye a la exposición global a la radiación.
Si se libera yodo radiactivo en el medio ambiente y penetra en el organismo por inhalación o ingestión, se concentrará en el tiroides aumentando el riesgo de cáncer de tiroides. El riesgo de cáncer de tiroides es mayor en los niños que en los adultos, en particular en los menores de 5 años y en aquellos cuyas dietas son generalmente carentes en yodo.
Medidas de protección de la salud en las emergencias nucleares
Durante las emergencias nucleares pueden aplicarse medidas de protección de la salud pública para limitar la exposición a la radiación y sus riesgos para la salud.
En la fase inicial de las emergencias (primeras horas o días) deben aplicarse medidas protectoras urgentes para prevenir la exposición a la radiación, teniendo en cuenta las dosis previsibles que se pueden haber recibido en el corto plazo (por ejemplo, dosis efectiva en 2-7 días, dosis tiroidea en una semana). Las decisiones se basan en las condiciones de las centrales nucleares, la cantidad de radiactividad real o potencialmente liberada a la atmósfera, las condiciones meteorológicas (por ejemplo, velocidad y dirección del viento, precipitación) y otros factores. Las autoridades locales pueden anunciar medidas urgentes como la evacuación, el refugio bajo techo o la administración de yodo no radiactivo.La evacuación es más eficaz cuando se utiliza como medida de precaución antes de una emisión a la atmósfera. El refugio bajo techo (por ejemplo, en casas, escuelas o edificios de oficinas) también puede reducir significativamente la exposición al material radiactivo liberado y dispersado.
La administración de yodo no radiactivo puede impedir la captación del yodo radiactivo por el tiroides. La toma de pastillas de yoduro de potasio antes o poco después de la exposición satura el tiroides de yodo y reduce la dosis de yodo radiactivo y el riesgo de cáncer de tiroides. Los comprimidos de yoduro de potasio no protegen de la radiación externa ni de otras sustancias radiactivas distintas del yodo.
Las pastillas de yoduro de potasio deben tomarse solo cuando así lo indiquen las autoridades competentes. Es importante seguir las recomendaciones de dosis, especialmente en los niños. Las embarazadas deben tomar pastillas de yoduro de potasio cuando así lo indiquen las autoridades competentes para proteger tanto su tiroides como el del feto. Cuando esté indicado, las mujeres lactantes también deben tomar pastillas de yoduro de potasio para protegerse a si mismas y proporcionar al lactante yoduro de potasio con leche materna.
Se pueden tomar medidas con respecto a los alimentos, el agua y la agricultura a fin de reducir la exposición a la radiación durante la fase inicial de una emergencia (por ejemplo, restricción del consumo de agua y de alimentos y lácteos de producción local).
El apoyo psicológico para paliar el estrés agudo tras un accidente nuclear puede acelerar la recuperación y evitar consecuencias a largo plazo, como el trastorno de estrés post-traumático u otros trastornos mentales persistentes. Las reacciones pueden ser intensas y prolongadas, y tener un impacto emocional profundo, sobre todo en los niños.
A medida que se vayan acumulando datos sobre la situación medioambiental y humana se pueden adoptar medidas de protección, como la reubicación de la población en viviendas temporales o, a veces, en reasentamientos permanentes. Estas medidas de protección se aplican teniendo en cuenta las dosis que puede recibir la población a largo plazo (por ejemplo, dosis efectiva a lo largo de un año). Deben establecerse programas de control de los alimentos y el agua para fundamentar decisiones a más largo plazo sobre la restricción de alimentos, el consumo de agua y el control del comercio internacional de productos alimentarios.La fase de recuperación puede durar bastante tiempo. El cese de las medidas de protección debe vincularse a los datos del control medioambiental, de los alimentos y de la salud humana, y basarse en análisis de los riesgos y beneficios. Deben establecerse programas apropiados de seguimiento a largo plazo para evaluar las consecuencias para la salud pública y la necesidad de medidas posteriores.
Fuente: http://www.who.int/mediacentre/factsheets/fs371/es/