Se debe distinguir desde un principio claramente
entre los conceptos de calor y energía interna de un objeto. El calor, (símbolo
Q), se define como la energía cinética total de todos los átomos o moléculas de
una sustancia. El concepto de calor, se usa para describir la energía que se
transfiere de un lugar a otro, es decir flujo de calor es una transferencia de
energía que se produce únicamente como consecuencia de las diferencias de
temperatura. La energía interna es la energía que tiene una sustancia debido a
su temperatura. La energía interna de un gas es esencialmente su energía
cinética en escala microscópica: mientras mayor sea la temperatura del gas,
mayor será su energía interna. Pero también puede haber transferencia de energía
entre dos sistemas, aún cuando no haya flujo de calor.

Por ejemplo, cuando un objeto resbala sobre una superficie hasta detenerse por efecto de la fricción, su energía cinética se transforma en energía interna que se reparte entre la superficie y el objeto (y aumentan su temperatura) debido al trabajo mecánico realizado, que le agrega energía al sistema. Estos cambios de energía interna se miden por los cambios de temperatura.
Cuando la ciencia termodinámica era incipiente, digamos a principios del 1800, y no se comprendía bien el concepto de calor, los científicos definieron el calor en términos de los cambios en la temperatura que el calor produce en los cuerpos.
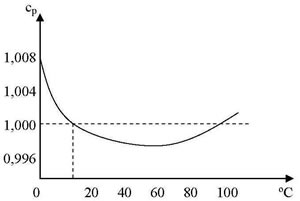
Por lo que se definió una unidad de medida del calor, llamada caloría, símbolo cal, como la cantidad de calor necesaria para elevar la temperatura de un gramo de agua en un grado Celsius desde 14.5º C a 15.5º C. La unidad de calor en el sistema ingles se llama Unidad térmica británica, (Btu), definida como la cantidad de calor necesaria para elevar la temperatura de una libra de agua en un grado Celsius de 63º F a 64º F. Se elige ese rango de temperatura, porque la cantidad de calor requerida depende levemente de la temperatura; se requiere más calor para elevar la temperatura del agua fría que la del agua a punto de hervir.

Cuando se describe el concepto de energía, se afirma que en cualquier
sistema mecánico siempre esta presente la fricción, por lo que siempre se
pierde energía mecánica y aparentemente no se conserva. Los experimentos demuestran
claramente que por efecto de la fricción, la energía no desaparece, sino que se
transforma en energía térmica. James Joule (inglés, 1818-1889) fue el primero
en establecer la equivalencia entre estas dos formas de energía. Joule encontró
que la energía mecánica que se transforma en calor, es proporcional al aumento
de temperatura. La constante de proporcionalidad, llamada calor específico, es
igual a 4.186 J/(g ºC). Se demuestra que una caloría, que se conoce como el
equivalente mecánico del calor, es exactamente igual a 4.186 J, sin importar
quien produce el aumento de temperatura:
1 cal = 4.186 J
Como en la actualidad se reconoce al calor como una forma de energía,
la unidad de medida de calor en el SI es el Joule, J. Algunas de las
conversiones más comunes entres las unidades de calor y energía son las
siguientes:
1 cal = 4.186 J = 3.97x10-3 Btu
1 J = 0.239 cal = 9.48x10-4 Btu
1 Btu = 1055 J = 252 cal
En nutrición se llama Caloría, Cal con mayúscula, a las calorías
alimenticias o dietéticas, usada en la descripción del contenido de energía de
los alimentos y equivale a 1000 calorías o 1kilocaloría, es decir 1 Cal = 1kcal
= 1000 cal.