Expresado en otras palabras, la Capacidad Calorífica ( C ) es la cantidad de energía necesaria para elevar en 1 °C la temperatura de una muestra determinada de material.
Si el cuerpo es de masa m, podemos definir algo que es característico de la sustancia o el material del cuerpo, y es lo que llamamos Calor Especifico ( c ). Basados en esta relación el calor seria Q=m.c.ΔT
El calor específico también de puede definir como la cantidad de calor que se debe suministrar a una unidad de masa determinada para elevarle la temperatura en 1 °C.
Para no confundir los dos términos el Calor Especifico se representa con la letra “c” minúscula y la Capacidad Calorífica con la letra “C” mayúscula.
Podemos asi encontrar un relación entre el calor especifico y la capacidad calorífica dada por c=C/m. Las unidades para el calor especifico pueden ser: cal/°C.g o J/Kg.°K
El calor específico del agua varía con la temperatura.
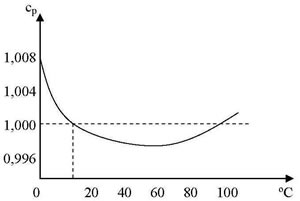
En la figura se ha representado la variación del calor específico del agua entre las temperaturas de 0 y 100 ºC, manteniendo la presión constante de 1 atmósfera.
Se puede observar que el valor es 1 en las proximidades de 15 ºC, debido a las forma escogida para definir la unidad de calor.
Tabla de calores específicos:

No hay comentarios:
Publicar un comentario